ABC do Tratamento
ESTABILIZAÇÃO DO CLORO
“O maior inimigo da verdade não é a mentira (deliberada, inventada e desonesta), mas o mito (persistente, persuasivo e irreal)”. Presidente John F. Kennedy
Rumores mal intencionados - e desprovidos de base técnica – apontam “riscos da utilização incorreta dos cloros estabilizados” e estão gerando dúvidas em consumidores desses produtos. Diga-se de passagem que a mesma tentativa tem sido empregada e periodicamente repetida por algumas empresas desde a década de 1970 – após o grande sucesso que os produtos dessa classe atingiram.
Quer saber a verdade? Veja as dúvidas mais frequentes e a verdade cientificamente comprovada sobre o uso de ácido cianúrico e seus derivados clorados (os cloros estabilizados) em piscinas:
É verdade que tanto o dicloro quanto o tricloro apresentam em sua composição o ácido cianúrico?
O dicloro isocianurato de sódio e a tricloro-s-triazina-triona (ou ácido tricloro isocianúrico) não são composições químicas (que pressupõem misturas de produtos químicos)* e sim produtos químicos puros, derivados do ácido cianúrico, com pesos moleculares definidos, como pode ser visto pelas fórmulas estruturais abaixo:
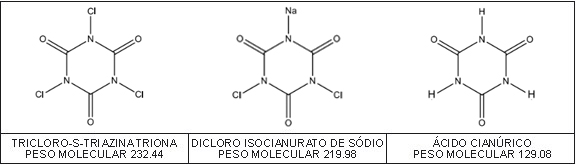
A reação do dicloro e tricloro com água resulta em ácido hipocloroso e ácido cianúrico, sendo que este é neutralizado e fica presente na água da piscina como um sal, geralmente de sódio ou de cálcio, dissociado em seus íons. O comportamento do cloro livre (ácido hipocloroso e íon hipoclorito), em soluções contendo ácido cianúrico ou seus derivados clorados (dicloro e tricloro), com pHs entre 7 e 8, é controlado principalmente pelos seguintes equilíbrios (reações químicas reversíveis)*1:
Para facilidade de entendimento, o anel cianúrico está representado como CA:
a) A partir de dicloro:
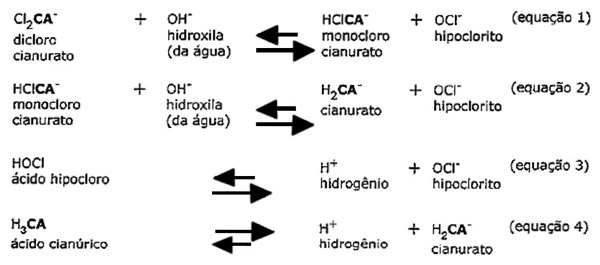
b) A partir de tricloro:
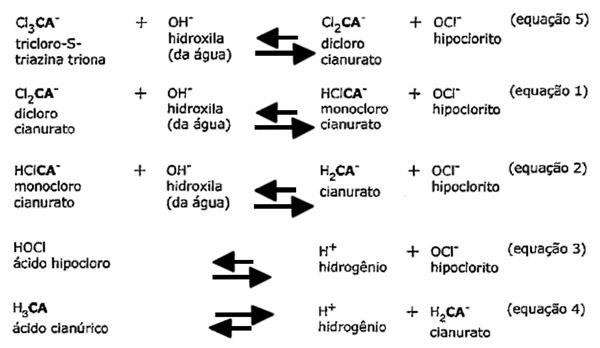
É sabido que o cloro, após ser aplicado na piscina, além de ficar exposto à radiação UV dos raios solares é consumido no seu processo de desinfecção da água. Por isso a aplicação do cloro tem de ser periódica na piscina a fim de mantê-la sempre saudável e protegida?
Outros fatores como pH e alcalinidade desajustados também contribuem no consumo do cloro?
O que é “aplicação periódica”? Uma vez por dia? Uma vez por semana: Uma vez por hora? Periodicamente é muito vago. Tecnicamente, pouco importa qual cloro você aplica na água, nem como e quando você aplica. O que importa mesmo para que a água se mantenha saudável e protegida é que, após atendida a sua demanda de cloro para oxidação e desinfecção das impurezas presentes, ela mantenha a presença de residual superior a 1 ppm de cloro livre (ácido hipocloroso) o tempo todo. A origem deste cloro pouco importa; nem a análise química da água consegue determinar a origem do ácido hipocloroso, isto é, ele pode provir de hipoclorito de sódio, do hipoclorito de cálcio, do cloro gás (adicionado ou gerado “in situ” a partir de sal e eletricidade), dicloro, do tricloro, ou de inúmeros outros produtos; o comportamento químico do cloro livre, o ácido hipocloroso, é exatamente igual, não importa sua origem (ver equação 3). Embora diversos fatores contribuam para o consumo residual de cloro livre, estima-se que 90% do cloro adicionado para desinfetar a água de piscinas não estabilizadas é dissipado em apenas 2 a 3 horas de exposição ao sol, enquanto que piscinas estabilizadas com 25 ppm de ácido cianúrico perdem apenas 30% de seu cloro, em igual período*2.
O conceito da estabilização com ácido isocianúrico e a desinfecção com isocianúricos clorados, introduzido nos E.U.A a partir de 1960 pela FMC, e no Brasil a partir de 1976 pela Genco, reduz significativamente a decomposição do residual de cloro livre pela luz ultravioleta, fazendo com que:
1. Mesmo com pequenas adições de cloro apenas uma vez por dia a água de piscinas residenciais se mantenha clorada por 24 horas na presença de luz solar, ou
2. Com apenas uma aplicação de tricloro em tabletes em cloradores flutuantes ou dosadores instalados em linha possa manter a água clorada continuamente por semanas ou até meses.
Exemplo 1*3: Veja na Figura 1 o resultado de teste realizado com dicloro granulado x hipoclorito de cálcio granulado: Diariamente, “as 6horas da manhã era adicionado a uma piscina a quantidade de hipoclorito de cálcio granulado recomendada na embalagem (aprovada pelo EPA-USA) para liberar 4,5 ppm de cloro livre (QUASE 7 GRAMAS/M³ DO PRODUTO!).Em outra piscina era adicionada a quantidade de dicloro granulado também aprovada pelo EPA-USA para liberar 1,5 ppm de cloro livre (MENOS DE 3 GRAMAS/M³ DO PRODUTO).
Resultado: 6 horas depois o residual de cloro na primeira piscina era zero, isto é a piscina ficava com 0 ppm de cloro das 12 horas até às 6 horas da manhã seguinte. Na segunda piscina o residual de cloro manteve-se 24 horas por dia entre 1 e 1,5 ppm, durante todo o período de duração do teste.
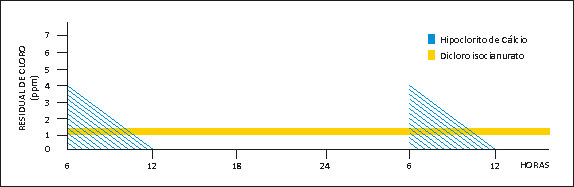
Exemplo 2 *4: Iniciado o teste foi adicionada a uma piscina não estabilizada a dosagem recomendada na embalagem de hipoclorito de cálcio granulado para prover residual de 4 ppm de cloro livre; em outra piscina de igual dimensão, porém estabilizada com 50 ppm de ácido cianúrico, foi adicionada a dosagem recomendada na embalagem dicloro granulado equivalente a cerca de 1 ppm de cloro livre. Os residuais de cloro de cada piscina foram analisados a cada 24 horas, antes de novas dosagens diárias dos mesmos produtos serem adicionadas. Ao fim de cada período de 24 horas a piscina tratada com hipoclorito de cálcio granulado não apresentava residual de cloro livre, mesmo duplicando, triplicando e quadruplicando a dosagem inicial do produto. No mesmo período, a piscina tratada com dicloro permanecia clorada, portanto sua dosagem foi reduzida para 50% após as primeiras 24 horas, para 40% da dosagem inicial ao fim de 48 horas e para 29% da dosagem inicial ao fim de 72 horas e a sua água ainda apresentava residual de 1 ppm de cloro livre ao fim do teste de 96 horas, conforme a tabela da Fig. 2.
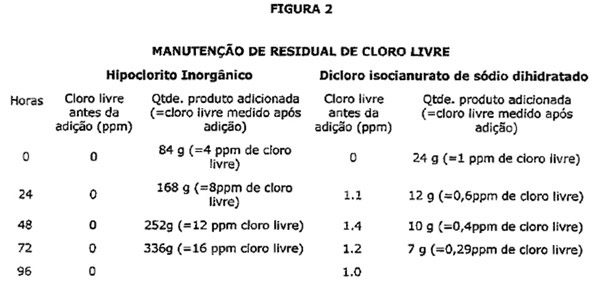
Tempo: sol a parcialmente nublado
pH: 7,2 a 7,9
Alcalinidade Total: 50 a 100 ppm
Volume da piscina: 18,93 m³
Temperatura da água: 19 a 23 ºC
É verdade que quando o dicloro e o tricloro são utilizados com regularidade a parcela que corresponde ao ácido cianúrico permanece na água, ou seja, o ácido cianúrico vai se acumulando na piscina e termina por provocar superestabilização (residual cerca de 100 ppm de ácido cianúrico)?
Não. O Anexo A (Chemical Operational Parameters) das normas americanas para tratamento de piscinas e spas*5,6,7,8,9,10, tanto residenciais como públicas, indica residuais ideais de ácido cianúrico entre 30 e 50 ppm e máximo de 150 ppm. Na Inglaterra é permitido o uso de dicloro, tricloro e ácido cianúrico, desde que o residual de ácido cianúrico não exceda 400 ppm*11. NOS E.U.A. a maioria dos órgãos de saúde estaduais aceitam residuais de até 100 ppm; alguns de até 200 ppm*12. Esses órgãos de regulação e normatização aceitariam tais residuais se isso fosse prejudicial à desinfecção? Uma revisão da eficácia bactericida dos isocianuratos*13 que incluiu inúmeros trabalhos científicos, teste de laboratório e de campo, concluiu que (1) o ácido cianúrico em residuais de pelo menos 200 ppm não afetam a eficiência bactericida do cloro e em alguns casos até a aumentam; (2) reduz significativamente a perda de cloro por ação de luz ultravioleta; (3) que os isocianúricos clorados são biocidamente ao menos equivalentes aos cloros orgânicos ou outros desinfetantes aceitos; (4) que o ácido cianúrico diminui o efeito bactericida do cloro em água destilada, mas que esse efeito se torna insignificante nas condições reais da água de piscinas; (5) que o nível do residual de cloro livre é o fator principal para manter desinfecção satisfatória e o mínimo de 1,0 ppm de cloro livre foi sugerido; (6) que o cloro combinado (cloraminas) é um desinfetante ineficiente e deve ser minimizado por supercloração frequente; (7) que a operação bem sucedida de piscina requer manutenção das faixas adequadas de parâmetros como pH e alcalinidade, que podem comprometer a eficácia biocida, e que em adição ao tratamento químico adequado, um bom sistema mecânico (bomba e filtro) é imprescindível, assim como manutenção contínua.
Ademais, qualquer circuito aquático fechado e sujeito a evaporação requer purga frequente para manter os sólidos totais dissolvidos sob controle, já que estes sim, quando em grande quantidade, podem diminuir a eficácia desinfetante, causar incrustações, turbidez, entre outros danos. Numa piscina, os sólidos totais se acumulam, não só devido ao aumento do teor de ácido cianúrico, mas de todos os produtos utilizados no tratamento (aliás, desinfetantes à base de cloro, os isocianúricos clorados, ao longo do tempo, são os que adicionam menor volume de sólidos torais dissolvidos e por isso requerem menor reposição de água nova para impedir o descontrole desse parâmetro*14), de excreções não oxidáveis de banhistas e pela evaporação da água. Resultados de estudos da eficiência bactericida do cloro frente ao acúmulo de sólidos totais e materiais não filtráveis e não oxidáveis provenientes de banhistas, em testes de campo realizados no Canadá*15, levaram as autoridades de saúde canadenses a aprovar regulamentação exigindo a reposição de 40 galões (151,4 litros) de água fresca, diariamente, para cada banhista nas piscinas sob sua supervisão. A diluição do acúmulo de sólidos só é possível pela reposição constante de água nova, prática saudável e obrigatória em qualquer sistema de tratamento de água de recirculação.
A piscina também está sujeita à perda normal de parte de sua água pelo uso por banhistas (splash out ou carry out), transbordamentos por chuvas (veja os índices pluviométricos) e a retrolavagem frequente dos filtros. Esta última é prática também obrigatória, que por si só impede um aumento do residual de ácido cianúrico na água e promove a diluição dos sólidos totais.
Num estudo em larga escala, com extensivos testes de campo realizados na Califórnia, E.U.A, diversas piscinas foram mantidas com dicloro isocianurato de sódio depois de estabilizadas com 50 ppm de ácido cianúrico, dentro dos padrões de tratamento normalmente aceitos, por um período de 6 meses; duas vezes por semana o residual de ácido cianúrico foi analisado e os testes mostraram que seu aumento máximo estabilizou-se em torno de 200 ppm em algumas piscinas, enquanto que a média situou-se em menos de 100 ppm*16. Testes de campo*17 realizados com diversos níveis de residuais de ácido cianúrico (0 a 300 ppm) em 30 piscinas, por 3 meses, demonstram que o nível de 300 ppm jamais pode ser atingido pelo uso normal de isocianúricos clorados (ácido cianúrico suplementar tinha de ser periodicamente adicionado manualmente porque seu residual tinha forte tendência a se estabilizar em níveis mais baixos).
É verdade que, ao ocorrer a superestabilização, a eficácia da sanitização fica reduzida, ou seja, ao realizar a análise da água, será constatada a presença de residual de cloro livre; porém, esta leitura não é real, uma vez que este residual de cloro livre se recombinará em parte com o excesso de ácido cianúrico, sendo que a reação de dissociação do dicloro e tricloro na água é reversível, impedindo a ação desinfetante do cloro que já não é mais “livre”, apesar de detectado como tal?
Não! Nos métodos colorimétricos para determinação do cloro livre, o reagente (ou indicador) mede tanto o ácido hipocloroso (HOCl e OCl- na equação 3) que está disponível, como os íons hipoclorito (OCl- nas equações 1, 2 e 5) que estão em equilíbrio com o anel cianúrico, que se constituem reserva do cloro livre disponível. Isso ocorre exatamente porque o equilíbrio entre o cloro livre (equação 3) e o cloro associado ao anel cianúrico é rapidamente restabelecido (princípio de Le Chatelier, para os químicos): à medida que o cloro livre da equação 3 reage com o indicador, ou seja, é consumido, novo cloro livre é formado pelos íons hipoclorito que estavam ligados ao anel cianúrico (equações 1, 2 e 5) para recompor o equilíbrio. A reação é reversível e essa liberação é imediata, tendo inclusive já sido calculada por Pinsky*18 como da ordem de 10-2 a 10-9 segundo por mol. Ou seja de 1/100 a 1/1.000.000.000 de segundo para cada cerca de 50 gramas de hipoclorito. Se a reposição do que está associado ao anel cianúrico é assim imediata, o cloro livre que está associado ao anel cianúrico deve ser considerado como livre. Então a análise do cloro livre revela, sim, o teor total de cloro livre presente na água, e todo ele está disponível. Aliás, a própria análise comprova a eficiência dos clorocianúricos em recompor rapidamente o cloro livre consumido.
É verdade que se pode comparar o uso dos cloros estabilizados com o de uma pessoa que toma antibiótico sem a real necessidade de tomá-lo e quando a necessidade real aparecer, ele não fará mais o efeito desejado? Com o ácido cianúrico proveniente do tricloro e do dicloro ocorre a mesma coisa?
Não! Trata-se de uma analogia infeliz que não cabe no assunto cloração ou oxidação, já que microorganismos e outros materiais orgânicos não conseguem desenvolver resistência contra esse método de eliminação (oxidação é queima!) como acontece com antibióticos. Se essa suposição fosse verdadeira, imagine que as florestas, após milênios de exposição a incêndios de toda espécie, teria hoje madeira totalmente incombustível.
O acúmulo do ácido cianúrico na água da piscina tornará mais fácil ao cloro adicionado reagir com ele, não combatendo os microrganismos quando a água estiver superestabilizada?
Não! Superestabilização não existe. Foi um mito criado por evidências circunstanciais, de diz-que-diz, citações fora de contexto e associação dos isocianúricos com cloraminas, em época (anos 60/70) que pouco se conhecia de sua química, do método de estabilização dos isocianúricos e de águas de piscinas, e alimentado por interessados em impedir o crescimento desses produtos (como ainda acontece hoje!). Todos os dados apresentados comprovam que os isocianúricos funcionam e se constituem a melhor opção para a desinfecção de águas de piscinas. São mais de 50 anos de sucesso crescente e ininterrupto junto a consumidores mais do que satisfeitos.
É verdade que a superestabilização da água permitirá também o desenvolvimento de algas, tornando a piscina esverdeada, e que quanto mais cloro (dicloro e tricloro) o usuário adiciona à piscina, mais verde ela fica e menor a eficácia do cloro livre detectado?
Não! Situações como as mencionadas não são devidas à presença de altos teores de ácido isocianúrico e sem a outros fatores sobejamente estudados, elucidados e documentados 14,15, 19 entre os quais podem ser citados metais dissolvidos, presença de algas, alta demanda de cloro, pH fora da faixa, excesso de cálcio, excesso de sólidos totais dissolvidos, filtração ineficiente etc., problemas comuns tanto em águas com isocianúricos como em águas sem isocianúricos.
É verdade que ocorrendo a superestabilização, a única solução possível para reduzir a concentração de ácido cianúrico é a drenagem parcial da água (às vezes total), o que implica em possíveis desvantagens: prejuízos para a estrutura da piscina, perda de milhares de litros de água e custos elevados para o consumidor?
Não! Quando parte ou toda a água da piscina é substituída por água nova parece que todo o problema se resolveu porque o ácido cianúrico foi descartado. Mas veja que também, as algas, os sólidos totais dissolvidos, o excesso de cálcio, e tudo mais que causava problema também foi diluído. A verdade é uma só: quando o teor de ácido cianúrico é elevado, isso indica que muito provavelmente o tratamento da água está sendo negligenciado, como retrolavagem dos filtros, reposição frequente de água nova, residual de cloro livre, pH e alcalinidade total, etc., por isso o teor de sólidos totais dissolvidos está também elevado e, consequentemente, se a eficácia da desinfecção está comprometida, nova adição de cloro não resolve o problema 14,19. Como já visto anteriormente, a reposição frequente de parte da água da piscina – que é parte intrínseca ao tratamento correto – mantém os sólidos dissolvidos dentro de um patamar estável de forma que esses problemas não ocorram.
É verdade que, como o próprio nome diz, o ácido cianúrico baixa o pH da piscina e o torna instável, sendo necessária a adição frequente de corretores de pH e que este normalmente é um custo extra que o usuário não percebe?
Não! Estamos falando do acúmulo de ácido cianúrico na água pelo uso de dicloro e tricloro – os isocianúricos clorados - em águas com pH de 7,2 a 7,8 e alcalinidade total de 100 a 120 ppm, o residual que fica na água é o de um sal de ácido cianúrico neutralizado; qualquer impacto que possa haver sobre o pH foi causado pelo isocianúrico clorado e não pelo ácido cianúrico. O termo “residual de ácido cianúrico” em águas de piscinas (pH 7,2 a 7,8) empregado erroneamente no mercado deve ser tecnicamente interpretado como “residual de sais de ácido cianúrico”, onde o que importa é o anel cianúrico em si. Wojtowicz¹ calculou as variações de pH causadas para a dosagem média para o tratamento de manutenção residual de cloro em um volume de água (com pH 7,5 – 80F – 100 ppm de alcalididade total e 100 ppm de ácido cianúrico) por uma semana com tricooro e com dicloro: as alterações foram respectivamente de -0,14 e -0,09, isto é o pH baixaria para 7,36 e 7,41 respectivamente, ou seja, ainda se situaria dentro da faixa ideal de 7,2 a 7,8.
Depois, o ácido cianúrico na verdade é um tampão (equilíbrio entre um ácido e seu sal) até melhor do que a própria alcalinidade total da água, já que sua capacidade máxima de tamponamento se situa em pH 6,8, enquanto que a do ácido carbônico (alcalinidade total) é de 6,3, isto é, a do ácido cianúrico está mais próxima do pH ideal de águas de piscinas (7,2 a 7,8)20. Para quem não sabe, tampão é uma solução de pH estável que tende a neutralizar qualquer variação de pH. Portanto, quanto maior a concentração de ácido cianúrico numa água, mais estável será seu pH.
É verdade que a forma mais inteligente para obter a estabilização do cloro na água da piscina é através da utilização de Estabilizante de Cloro (ácido cianúrico – 50g para cada 1000 litros de água) de uma única vez, caso contrário a superstabilização é inevitável e que a aplicação em quantidades adicionais/complementares de Estabilizante de Cloro na piscina deverá ocorrer somente nos casos em que houver necessidade de reposição de grandes volumes de água, eliminada nos processos de retrolavagem de filtros e/ou drenagem?
Não! A estabilização com 50 ppm de ácido cinaúrico deve ser feita em todas as piscinas expostas ao sol, no início do tratamento. Quando se utilizar cloros não estabilizados na cloração diária será necessário analisar, ao menos uma vez por mês, o residual de ácido cianúrico e recompor o nível inicial de 50 ppm para manter a estabilização eficiente. Quando se utilizar um cloro estabilizado, essa reposição é desnecessária e o residual de ácido cianúrico nunca atingirá residuais elevados.
Em qualquer caso, mantido o residual ideal de 2 a 4 ppm de cloro livre na água o tempo todo, pH de 7,2 a 7,8, alcalinidade total de 80 a 120 ppm e mantendo-se as demais práticas do bom tratamento, como retrolavagem dos filtros, limpeza das bordas, a desinfecção da água se processará normalmente (não importa o tipo de cloro utilizado), não haverá acúmulo de sólidos totais dissolvidos e o uso da piscina poderá ser feito com toda a segurança.
Os cloros estabilizados dicloro e tricloro podem ser utilizados para desinfecção de água para consumo humano?
Sim. Os produtos dicloro e tricloro devidamente registrados na ANVISA para esse fim podem ser utilizados em sistemas de tratamento de água para consumo humano de uso contínuo. A Norma ABNT:NBR 15.784:2009 - “Produtos químicos utilizados no tratamento da água para consumo humano – efeitos à saúde – Requisitos” 21, inclui tanto o dicloro isocianurato de sódio como o ácido tricloroisocianúrico como produtos destinados à desinfecção e oxidação no tratamento de águas para consumo humano. Esses produtos são atualmente utilizados por companhias públicas de saneamento, indústrias, granjas e agropecuária.
Órgãos internacionais como a NSF/ANSI-60, Drinking water treatment chemicals – Health Effects 22 (Produtos químicos para tratamento de águas – Efeitos à Saúde) certificam esses produtos para tratamento de águas para consumo humano. Além disso a OMS, “Guidelines for drinking water quality, World Health Organization também menciona o dicloro e tricloro para tratamento de água para consumo humano.
Como se vê pelo exposto, existe hoje um acervo inestimável de conhecimento técnico, baseado em ciência, pesquisas de laboratório e de campo, e sobretudo resultado da aplicação dos produtos dicloro e tricloro pelos consumidores, desenvolvidos ao longo de mais de 50 anos de história, mas ainda assim os métodos de combate a esse sucesso continuam sendo a malícia, a futrica, a mentira com a criação de mitos e dúvidas na cabeça de usuários incautos.
REFERÊNCIAS:
1. Swimming Pool Water Balance, Part 1: The Effect of Cyanuric Acid and Other Interferences on Carbonate Alkalinity – de John A. Wojtowicz – in Journal of the Swimming Pool and Spa Industry, Vol. 1, Nº 1, pgs. 7-13.
2. Cyanuric Acid, It’s Use and Control in Swimming Pools – Special Report Nº 7858 – Research and Development, Inorganic Chemical Division, Monsanto Company – by G.D. Nelson – April 7th, 1972, pgs. II-1.
3. FCM Technical Report – 010679SKJ.
4. FCM Technical Report – ICG 11/B.
5. ANSI/NSPI-1/1991 – AMERICAN NATIONAL STANDARD INSTITUTE.
6. ANSI/NSPI-2/1992 – AMERICAN NATIONAL STANDARD INSTITUTE.
7. ANSI/NSPI-3/1992 – AMERICAN NATIONAL STANDARD INSTITUTE.
8. ANSI/NSPI-4/1999 – AMERICAN NATIONAL STANDARD INSTITUTE.
9. ANSI/NSPI-5/1995 – AMERICAN NATIONAL STANDARD INSTITUTE.
10. ANSI/NSPI-6/1992 – AMERICAN NATIONAL STANDARD INSTITUTE.
11. Carta ref. WS/330/163, de 07/02/1977, do Department of the Environment, Londres, Inglaterra.
12. A Review of Mwthods for Testing Cyanuric Acid Residuals in Swimming Pool Water – de Mary Constanzo – in Proceedings Vol. III – NSPI Chemistry Simposium (Advances in Pool and Spa Water Chemistry – Analisys, Measurement and Testing – 1998).
13. The Bacterial Efficacy of Cyanurates, A Review – F.W. Linda, R. C. Hollenbach – in Journal of Environmental Health, Vol.40, Nº 6, May/Jun 1978, pgs. 324-329.
14. Problems os Pool Water Management – G.D. Nelson, F.B. Clarke e R. Kimerle– apresentado na Convenção de 1973 do NSPI em Las Vegas, Nevada, USA.
15. Recirculating and Overflow Refill of Public Swimming Pools: A Chemical and Microbiological Appraisal, de D.M McLean, R. Brown Jr. e M.C Nixon – in Canadian Journal of Public Health, 53, January 1962, pgs.9-16 .
16. FMC Report T-76-122, 1973 California Swimming Pool Field Study.
17. FMC Technical Report ICD/T – 74-038 – Determination of Swimming Pool Economics with Various Sanitizers in Stabilized and Unstabilezed Pools, de R.C. Hollenbach.
18. FMC Technical Report ICD/T – 76-130 – Hydrolysis of the Clorinated S-trizinetriones – de M.L. Pinsky.
19. The Enigma of Total Dissolved Solids, F.W. Linda, R.C. Hollenbach, apresentado na Convenção annual de 1976 (14/11/1976) do National Swimming Pool Institute, em Chicago, Illinois, USA.
20. Swimming Pool Water Buffer Chemistry – de John A. Wojtowicz – in Journal of the Swimming Pool and Spa Industry, Vol. 3, Nº 2, pgs. 34-41.
21. ABNT NBR 15784 – Segunda Edição (24/02/2014) – Produtos Químicos Utilizados no Tratamento de Água para Consumo Humano – Efeitos à saúde – Requisitos. 22. NSF/ANSI60, Drinking water treatment chemicals – Health Effects, 2005.
São Paulo, 18 de Setembro de 2015.
Alcides dos Santos Lisboa
Responsável Técnico – CRQ IV nº: 04405984



